Rozuvastatino poveikis aterosklerozinių plokštelių stabilumui
14. 1. 2023

Aterosklerozė yra dažniausia ir svarbiausia širdies ir smegenų kraujagyslių ligų priežastis. Dešimtmečius ji gali progresuoti slapta, kol pradeda reikštis simptomais ir aterotrombozinėmis komplikacijomis. Simptominė aterosklerozinė liga dažniausiai rodo, kad histopatologiniai kraujagyslių pažeidimai yra gilūs ir jau beveik ar visiškai negrįžtami. Todėl labai svarbu anksti pradėti aterosklerozės, dar subklinikinės, gydymą ir jos rizikos veiksnių valdymą, kol neatsirado klinikinių ligos simptomų.
Aterosklerozė yra liga, kurios atsiradimą lemia daugelis veiksnių, bet vienas svarbiausių – serumo lipidų kiekio padidėjimas ir disbalansas įsivyraujant aterogeniškoms lipidų frakcijoms. Padidėjus mažo tankio lipoproteinų (MTL) koncentracijai kraujyje cholesterolis sparčiau patenka po kraujagyslių endoteliu ir tai lemia aterosklerozinių plokštelių (ateromų) augimą. Vienos ateromos yra stabilesnės ir rečiau sukelia ūminius vainikinių arterijų sindromus (ŪVAS) nei kitos. Būtent nestabilių ateromų plyšimas paleidžia trombų susidarymo kraujagyslėje mechanizmą, kuris patogeneziškai susijęs su miokardo infarktu, išeminiu insultu ir kitokiais kardiovaskuliniais įvykiais.
Statinai yra pirmojo pasirinkimo ir efektyviausi vaistai hipercholesterolemijai ir dislipidemijai gydyti. In vitro tyrimų duomenimis, statinai, be antilipidinio, turi ir kitokių gretutinių, pleotropinių, poveikių: gerina endotelio veiklą ir didina jo apsaugą, reguliuoja krešumo faktorių aktyvumą, mažina uždegimą, veikia antioksidantiškai. Statinai ne tiktai slopina aterosklerozinių plokštelių (ateromų) susidarymą, bet ir stabilizuoja jau esančias ateromas, mažina jų plyšimo riziką. JUPITER tyrimo duomenimis, palyginti su placebu, 20 mg/d. rozuvastatino 44 proc. sumažino kardiovaskulinių išeičių, įskaitant mirčių, dažnį, bet nepadidino tokių nepageidaujamų poveikių, kaip miopatija, kepenų pažeidimas ar piktybiniai navikai, rizikos.
Visų statinų poveikio mechanizmai slopinant MTL cholesterolio sintezę kepenyse bei stabilizuojant ateromas yra panašūs, tačiau aktyvumas ir gaunamas rezultatas skiriasi. Paskelbti keli tyrimai, nagrinėjantys skirtingų statinų poveikį stabilizuojant aterosklerozines plokšteles.
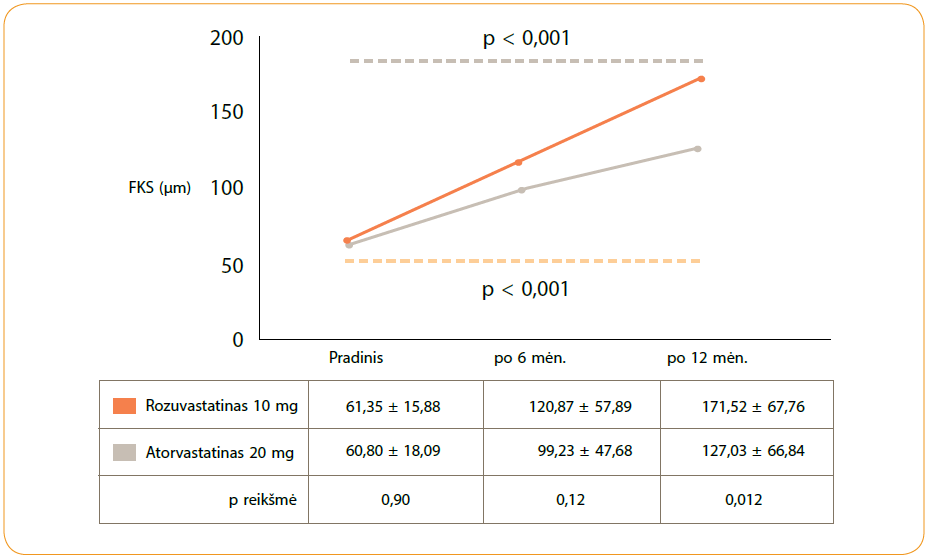
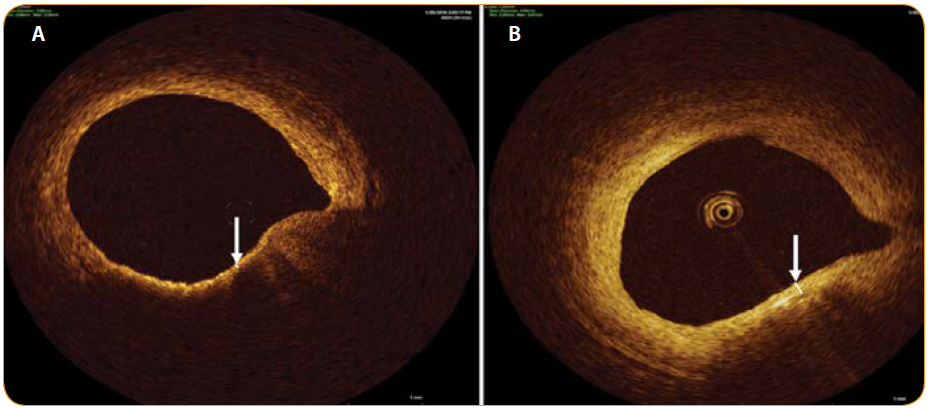
tyrime paciento fibrozinës kepurëlës storis siekë 50 ?m (balta rodyklë), B. po 12 mën. gydymo rozuvastatino
fibrozinës kepurëlës storis siekë apie 300 ?m (balta rodyklë)
Statinai ir aterosklerozinių plokštelių kepurėlių storis
V. Thondapu su bendraautoriais atliko tyrimą Comparison of Rosuvastatin versus Atorvastatin for Coronary Plaque Stabilization, kuriame dalyvavo pirmą kartą gyvenime diagnozuota išemine širdies liga sergantys pacientai. Vidutinis tyrimo dalyvių amžius buvo 56,1 m., 63 proc. sudarė vyrai. Tyrimu buvo siekiama ištirti vainikinių arterijų plokštelių atsaką į gydymą skirtingais statinais, naudojant serijinį multimodalinį intrakoronarinį vaizdą.
Pacientai, kuriems reikėjo atlikti vainikinių arterijų intervencijas, buvo atsitiktinai suskirstyti į dvi grupes: vieniems skirta 10 mg rozuvastatino per parą, kitiems – 20 mg atorvastatino. Optinė koherentinė tomografija ir vidukraujagyslinis ultragarsas buvo atliekami tyrimo pradžioje, po 6 mėnesių ir po 12 mėnesių. Optine koherentine tomografija buvo siekiama nustatyti plonasluoksnes fibroateromas, ateromų kepurėlių storį ploniausiose vietose, lipidinės šerdies storį ir jos ilgį. Bendras ir procentinis ateromos tūris buvo išanalizuoti vidukraujagysliniu ultragarsu.
Abiejose grupėse per pirmuosius šešis mėnesius bendrojo cholesterolio ir MTL cholesterolio kiekis reikšmingai sumažėjo, o nuo 6 iki 12 mėnesių reikšmingai nesikeitė. Tyrimo pabaigoje MTL cholesterolio koncentracija rozuvastatino grupėje buvo pasiekta 1,9 mmol/l, o atorvastatino grupėje – 2,0 mmol/l. Didelio tankio lipoproteinų koncentracija tyrimo laikotarpiu reikšmingai nepasikeitė ir jokio skirtumo tarp gydymo grupių nebuvo.
O štai rozuvastatino ir atorvastatino poveikis aterosklerozinių plokštelių parametrams skyrėsi. Tyrimo laikotarpiais iki 6 mėnesių ir iki 12 mėnesių minimalus ateromų fibrozinės kepurėlės storis nuosekliai ir reikšmingai padidėjo abiejose grupėse. Rozuvastatino grupėje fibrozinės kepurėlės storis didėjo labiau – nuo 61,4 µm tyrimo pradžioje iki 171,5 µm tyrimo pabaigoje, atorvastatino grupėje fibrozinė kepurėlė pastorėjo nuo 60,8 µm iki 127,0 µm. (1 pav.). Ateromų su plona kepurėle skaičius rozuvastatino ir atorvastatino grupėje sumažėjo per pusę (2 pav.).
Nustatyta, kad tik rozuvastatinas sumažino makrofagų tankį ir smulkiųjų kraujagyslių skaičių ateromose (atitinkamai 32 ir 47 proc.). Bendrasis ateromos tūris rozuvastatino grupėje sumažėjo statistiškai patikimai nuo 109,2 mm3 iki 102,5 mm3 (p = 0,04), tačiau atorvastatino grupėje sumažėjimas nuo 83,3 mm3 iki 77,9 mm3 nepasiekė statistinio patikimumo (p = 0,07).
Tyrimo autoriai padarė išvadą: 10 mg per parą rozuvastatino ir 20 mg atorvastatino panašiai vienodai sumažino serumo lipidų kiekį, tačiau rozuvastatinas greičiau ir efektyviau stabilizavo ateromines plokšteles, labiau sumažino ateromų tūrį. Dauguma ŪVAS įvyksta plyšus nestabiliai ir lengviau pažeidžiamai aterosklerozinei plokštelei. Plokštelės plyšimo rizika didesnė, jei yra:
- plona fibrozinė ateromos kepurėlė;
- didelė nekrozinė šerdis;
- padidėjęs makrofagų kiekis ateromoje;
- vyksta ateromos remodeliacija (kaip kompensacinis mechanizmas);
- ateromoje formuojasi naujadarinės kraujagyslės.
Šie ateromų požymiai ir kitimai gali būti vizualizuojami vidukraujagyslinės echoskopijos ir optinės koherentinės tomografijos metodais.
Plona fibrozinė kepurėlė yra vienas svarbiausių ateromos pažeidžiamumo požymių. Tyrime per 12 mėnesių rozuvastatino grupėje fibrozinės kepurėlės storis padidėjo apie 3 kartus, o atorvastatino grupėje – 2 kartus.
Mažo tankio lipoproteinų cholesterolio (MTL Ch) kiekis abiejose grupėse labiausiai sumažėjo per pirmuosius 6 tyrimo mėnesius, o paskui mažai keitėsi, bet ateromų stabilizacija vyko toliau, nors MTL Ch kiekis nebemažėjo.
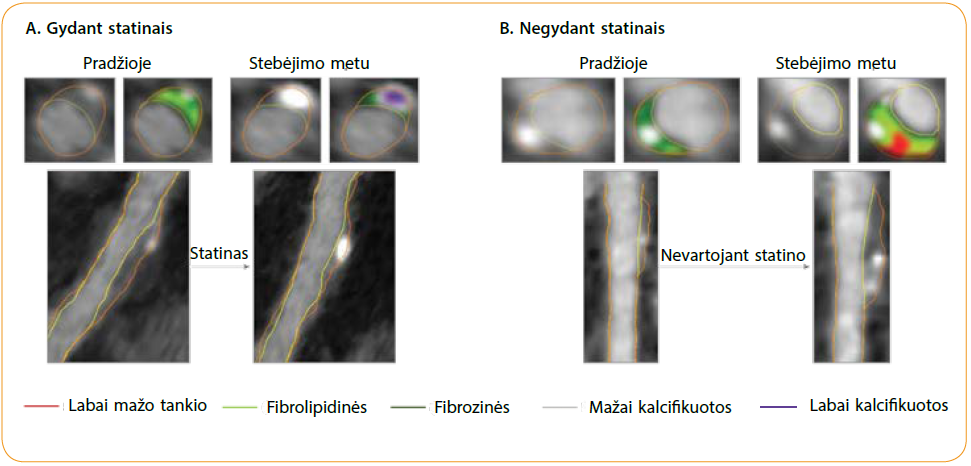
Statinai ir aterosklerozinių plokštelių struktūriniai pokyčiai
Atliekant ankstesnius tyrimus buvo rasta, kad ŪVAS sirgę asmenys turi santykinai mažiau labai kalcifikuotų plokštelių, palyginti su nesirgusiais ŪVAS. Iškelta hipotezė, kad viena priežasčių, kodėl statinų terapija sumažina ŪVAS riziką, gali būti ta, kad statinai skatina jau esamų lipidinių plokštelių kalcifikaciją.
Šiai hipotezei patvirtinti R. R. Alexanderis su bendraautoriais, pasitelkę vainikinių arterijų kompiuterinės tomografijos angiografiją, analizavo statinų poveikį įvairių tipų aterosklerozinėms plokštelėms – tyrimo pavadinimas Association of Statin treatment with Progression of Coronary atherosclerotic Plaque Composition.
Buvo nagrinėjamas aterosklerozinių plokštelių sudėties kitimas vainikinėse kraujagyslėse. Šeši ateromų sudėties tipai buvo apibrėžti pagal kompiuterinėje tomografijoje naudojamą radiotankį, išreikštą Hounsfieldo vienetais (HV): minkštos riebalinės (–30–75 HV), fibrolipidinės (76–130 HV), fibrozinės (131–350 HV), mažai kalcifikuotos (351–700 HV), labai kalcifikuotos (701–1000 HV) ir labai didelio tankio (> 1000 HV) ateromos. Duomenų analizė buvo atlikta nuo 2019 m. rugpjūčio mėn. iki 2020 m. kovo mėn. Į tyrimą buvo įtraukti 2 458 vainikinių arterijų pažeidimai 857 pacientams (vidutinis amžius 62 metų; 63 proc. buvo vyrai; 63,9 proc. pacientų buvo gydomi statinais).
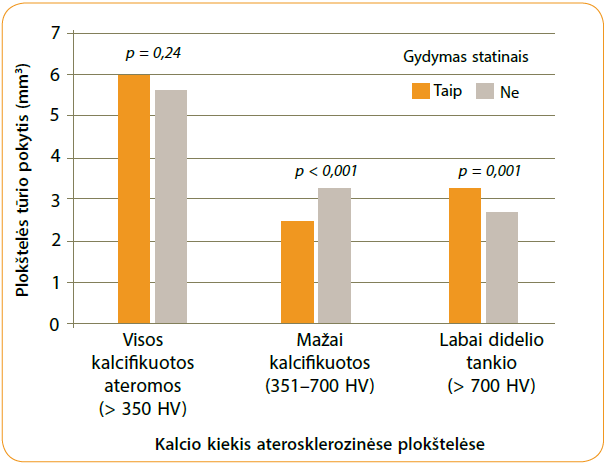
Gydymas statinais buvo susijęs su minkštų riebalinių ir fibrolipidinių plokštelių tūrio mažėjimu bei labai kalcifikuotų ir labai didelio tankio plokštelių greitesniu progresavimu – statinų vartojimas buvo susijęs su spartesniu išeminės širdies ligos progresu į labiau kalcifikuotų ateromų fazę (3 pav.). Nagrinėjant vien tik kalcifikuotas ateromines plokšteles rasta, kad vartojant statinus nedidėja ateromų tūris, bet vyksta jų transformacija – kaupiasi kalcis, jis tampa tankesnis. Šis tyrimas parodė, kad aterosklerozės progresavimą galima stabdyti ir keisti skiriant statinų terapiją. Veikiant statinams, vainikinėse kraujagyslėse mažėjo minkštųjų riebalinių ir fibrolipidinių plokštelių, kurios linkusios plyšti ar išopėti, ir daugėjo stabilesnių kalcifikuotų plokštelių. O neskiriant statinų vainikinių arterijų pažeidimai laikui bėgant vis didėjo (4 pav.).
Kodėl statinų vartojimas skatina ateromų kalcifikaciją? Naujausi tyrimai duoda pagrindo manyti, kad toks statinų poveikis susijęs su makrofagų Rac1–interleukino 1– beta ašies moduliacija. Formuojantis ir progresuojant aterominei plokštelei, jos nekrozinėje šerdyje esantys makrofagai ir lygiųjų raumenų ląstelės žūsta, išsiskiria laisvas kalcis ir kalcio fosfatas, kurie kristalizuojasi ir sudaro mikrokalcifikatus. Mikrokalcifikatai jungiasi į fragmentus, kurie paskui suformuoja didesnius tankaus kalcio lakštus – jie atliekant vainikinių arterijų kompiuterinės tomografijos angiografiją aptinkami kaip tankiai kalcifikuotos aterominės plokštelės.
Ankstesniais tyrimais nustatyta, kad rozuvastatinas gali sumažinti endotelio ir monocitų matricos metaloproteazių koncentraciją, stabdyti ateromos kepurėlės plonėjimą ir stabilizuoti aterosklerozinę plokštelę. Šiuos procesus lydi makrofagų kiekio ateromoje mažėjimas, kurį skatina rozuvastatinas. Keliama prielaida, kad rozuvastatinas kliniškai reikšmingai mažina su makrofagais ir monocitais susijusį kraujagyslių sienelių uždegimą, todėl aktyviau stabdo aterosklerozės vystymąsi.
Išvados
Kuo didesnio tūrio yra aterosklerozinės plokštelės, tuo jos mažiau stabilios, labiau linkusios išopėti ir plyšti, kas „užveda“ trombogenezės kaskadą, sukelia kraujagyslių trombozę, vainikinių arterijų okliuziją, nestabiliąją krūtinės anginą, miokardo infarktą, išeminį insultą ar mirtį. Gydymas statinais stabdo ateromų tūrio didėjimą, o didelėmis dozėmis net sukelia ateromų regresiją. Taip pat vartojant statinus didėja ateromų kepurėlių storis, jos tampa stabilesnės. Be to, gydymas statinais skatina ateromų tankio didėjimą ir kalcio kaupimąsi. Ši tendencija vertinama palankiai, nes aterosklerozinių plokštelių kalcifikacija mažina ūminių vainikinių arterijų sindromų riziką: kuo plokštelė labiau kalcifikuota, tuo ji stabilesnė ir yra mažesnė plyšimo rizika. Rozuvastatinas yra veiksmingas statinas, stabilizuojantis aterosklerozines plokšteles.